Bruxismus und Osteopathie
Zusammenfassung
Bruxismus kann sowohl als Wach- (WB) wie als Schlafbruxismus (SB) auftreten. Die Prävalenz differiert je nach Untersuchungsmethode und wird bei WB mit 22,1–31% und bei SB mit 12,8±3,1% angegeben. Die Ätiologie des Bruxismus ist nur unvollständig bekannt, jedoch ist von einem multifaktoriellen Geschehen auszugehen. In diesem Artikel werden die Risikofaktoren vorgestellt. Des Weiteren werden neuroevolutionäre und paläoanthropologische Perspektiven erläutert und Einblicke in die Diagnostik gegeben. Zuletzt werden Behandlungsansätze beschrieben und das LEIT-Reset vorgestellt, bei dem extrinsische (osteopathisch manuelle Techniken – OMT) und intrinsische Kiefertechniken (Selbsthilfetechniken) aufeinander abgestimmt angewendet werden.
Schlüsselwörter
Wachbruxismus, Schlafbruxismus, kraniofazialer Schmerz, primärer Kopfschmerz, Kiefergelenkstörung, Zähneknirschen, Bruxismus, Zahnhartsubstanz, Manualtherapie, craniomandibuläre Dysfunktion (CMD), osteopathisch manuelle Techniken, OMT, LEIT-Reset, Selbsthilfetechniken
Summary
Bruxism can occur both as waking bruxism (WB) and as sleep bruxism (SB). The prevalence differs according to the method of investigation and is reported to be 22.1–31% in WB and 12.8±3.1% in SB. The etiology of bruxism is not completely known, but a multifactorial cause can be assumed. In this article, the risk factors are presented. Furthermore, neuroevolutionary and paleoanthropological perspectives are outlined and insights into diagnostics are given. (Manual therapy) treatment approaches and self-help techniques for patients are described. Finally, treatment approaches are described and the LEIT-Reset is presented – in which extrinsic (osteopathic manual techniques, OMT) and intrinsic jaw techniques (self-help techniques) are applied in a coordinated way.
Keywords
awake bruxism, sleep bruxism, craniofacial pain, primary headaches, temporomandibular disorder (TMD), tooth grinding, bruxism, hard dental tissue, osteopathic manual technics (OMT), craniomandibular dysfunction (CMD), LEIT-Reset, self-help techniques.
Grundsätzlich wird zwischen dem Wachbruxismus (WB) und dem Schlafbruxismus (SB) unterschieden. Im wachen Zustand äußert sich der Bruxismus durch Zähnereiben oder -knirschen, im Zusammenpressen der Zähne oder durch spontane Bewegungen des Unterkiefers ohne Zahnkontakt [88]. Diese Symptome treten laut Literaturangaben bei ca. 20% der erwachsenen Bevölkerung auf [47] und können sowohl bei Erwachsenen als auch bei Kindern Kiefer-, Kaumuskel- oder Kopfschmerzen nach sich ziehen. Eine Metaanalyse hat ergeben, dass 1/6 der Kinder und Jugendlichen klinische Kiefergelenkbeschwerden aufweisen und über 23% der Vorschulkinder von Zähnepressen- oder reiben und pathologischen Kiefergelenkgeräuschen betroffen sind [83]. Obwohl die Pathogenese des WB noch unbekannt ist, gelten Stress, Ängste und nervöse Tics als Risikofaktoren [47].
Der Schlafbruxismus ist definiert durch das Auftreten der o.g. Kaumuskelaktivitäten während der Schlafphase. Dabei wird weiter zwischen rhythmischen bzw. phasischen und nicht-rhythmischen (kurze, repetitive Kontraktionen der Kaumuskulatur mit mehr als 3 Muskelkontraktionen von 0,25–2 sec) bzw. tonischen (Muskelkontraktionen >2 sec) Aktivitäten unterschieden. Weiterhin stellt SB nach der ICD10-Klassifizierung keine Bewegungs- oder Schlafstörung bei ansonsten gesunden Menschen dar.
Bruxismus kann weiters in primär (eigenständig) und sekundär (durch andere Faktoren bedingt) differenziert werden. Sekundärer Bruxismus kann infolge von Medikamenten (Antidepressiva, Antikonvulsiva, Antipsychotika, Antihistaminika, dopaminerge, kardioaktive Medikamente) oder Drogen (v.a. Rauchen, Alkohol, Amphetamine, Kokain), aber auch als Komorbidität bestimmter Erkrankungen (v.a. Koma und Schädel-Hirn-Trauma) auftreten [88].
Relevanz
Während der sekundäre Bruxismus behandelt werden kann, gilt der primäre Bruxismus derzeit als nicht heilbar. Dies stellt verschiedene Disziplinen vor große Herausforderungen, denn es kann infolge von Bruxismus zu Zahnhartsubstanzverlusten und ggf. zu einem Verlust von Zahnersatz und/oder -füllungen kommen. Somit gilt er als Risikofaktor für ein frühzeitiges Versagen von zahn- und kieferorthopädischen Interventionen [88].
Prävalenz
Die Angaben über die Prävalenz von Bruxismus fallen aufgrund der verwendeten diagnostischen Methode (Anamnese, klinische Untersuchung, instrumentelle Erfassung) sehr variabel aus. In der S3-Leitlinie „Diagnostik und Behandlung von Bruxismus“ wird die Prävalenz von WB mit 22,1–31% und bei SB mit 12,8±3,1% angegeben [88]. In der Regel nimmt die Prävalenz mit dem Alter ab und zeigt keine belastbare geschlechtsspezifische Verteilung [74]. Eine systematische Überprüfung ergab sehr starke Variationen von Prävalenzraten von SB bei Kindern (2,5–56,5%) [88], u.a. aufgrund der unterschiedlich untersuchten Altersgruppen. Tritt Bruxismus bereits im Kindesalter auf, steigt das Risiko, dass auch im späteren Leben der Bruxismus bleibt.
Ätiologie
Teilweise ist die Ätiologie des Bruxismus nicht bekannt, jedoch ist von einem multifaktoriellen Geschehen auszugehen [69].
In der Ätiologie von Bruxismus kann zwischen peripheren und sekundären Faktoren unterschieden werden. Zu den peripheren Faktoren gehören z.B. der Zahnschluss oder die Morphologie des Schädels und Kiefers, insbesondere im Wachstum, welche nach aktuellem Forschungsstand dem sekundären Bruxismus zugeschrieben werden. Daraus wird geschlussfolgert, dass periphere Faktoren in keiner ätiologischen Beziehung mit primärem Bruxismus stehen [60]. Derzeit wird von einer übergeordneten Rolle verschiedenen zentraler Faktoren ausgegangen. Dazu zählen emotionaler Stress, Angststörungen, Schlafstörungen (z.B. Insomnie), physiologische, biologische und genetische Faktoren, neurochemische Transmitterfehlregulationen oder Nikotin-, Alkohol- oder Drogenabusus [88]. Systematische Literaturanalysen haben ergeben, dass WB eher mit psychologischen Faktoren, wie emotionalem Stress, assoziiert ist, während bei SB von einer zentralnervösen Fehlregulation ausgegangen wird [5], [19], [20], [37], [67], [68].
Risikofaktoren
Belastbare, evidenzbasierte Ergebnisse aus longitudinalen Studien zur abschließenden Identifikation von Risikofaktoren stehen noch aus. Im Folgenden werden die diskutierten Faktoren vorgestellt.
Die Summation der genannten Risikofaktoren erhöht das Risiko für dysfunktionellen Schlafbruxismus.
Neuronale Risikofaktoren – Beim SB bleibt die Ätiologie bisher ungeklärt, während der okklusale Kontakt der Zähne im Ober- und Unterkiefer anscheinend nur eine untergeordnete Rolle einnimmt. Vielmehr scheint SB mit Microarousal-Zuständen im Schlaf assoziiert zu sein, d.h. es kommt zu einem Anstieg der autonomen Herz- und Atemaktivität sowie zu nichtintentionalen Bewegungen im Schlaf. Schlafmedizinisch betrachtet stellt der SB eine schlafbezogene Bewegungsstörung dar [47]. Weiter ist ein Zusammenhang von Kaubewegungen, insbesondere bei nicht-nutritivem Kauen, und dem Hippocampus bekannt (Abb. 1) [15].
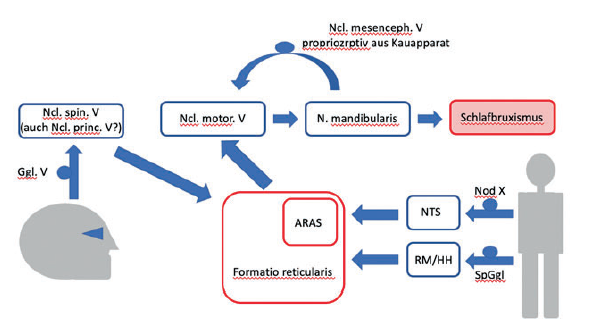
Abb. 1: Neuronale Einflüsse beim Schlafbruxismus (aus [52] mit freundlicher Genehmigung). Nod=Ganglion nodosum (inferius nach neuer Nomenklatur) des Vagus. Strenggenommen müsste auch das Ggl. jugulare (superius) genannt werden, da Afferenzen aus dem oberen Aerodigestivtrakt, deren Zellkörper im Ggl. jugulare liegen, auch ein Microarousal auslösen könnten. (ARAS=aufsteigendes retikuläres Aktivierungssystem).
NTS= Ncl. tractus solitarii
RM/HH= Rückenmark/Hinterhorn
SpGgl= Spingalganglion
Schlafstörungen – Zu den bekannten auftretenden Schlafstörungen bei Bruxismus zählen Albträume bei Kindern [4], gestörter Schlafrhythmus bei Schichtarbeiter*innen [3], Insomnie [22], Schnarchen [66] und Schlafapnoe [39]. Des Weiteren ist bekannt, dass das unbewusste Zähnepressen in den Minuten vor dem Rapid-Eye-Movement-Schlaf (REM-Schlaf) am stärksten ausgeprägt ist, was auf einen Einfluss der Schlafstadien auf SB hindeutet. Im Schlaf treten physiologische rhythmische Kaumuskelaktivitäten (RMMA) bei ca. 60% der gesunden Bevölkerung auf. RMMA sind definiert als langsame (1 Hz) kauende Bewegungen ohne Auftreten von Zahnschleifen. Bei Betroffenen treten diese rhythmischen Kaumuskelaktivitäten etwa 3× öfter und bis zu 1/3 intensiver auf [48]. RMMA während des Schlafs geht mit einer vorübergehenden Aktivierung von kortikalen, limbischen und autonomen Schaltkreisen einher [15]. Die Bewegungen des Kiefers werden durch eine kortikal-autonome Herzaktivität durch den Sympathikus induziert [75]. Zudem werden der Lobus temporale sowie das limbische System bei Kieferspannung mit anschließendem Kieferpressen aktiviert [15].
Psychologische und verhaltensbezogene Risikofaktoren – Emotionaler Stress wird v.a. bei Kindern als ätiologischer (Risiko-)Faktor diskutiert [34], [38]. Eine evidenzbasierte Aussage wird über die Methodik der Elternbefragung erschwert.
Folgende Stressoren korrelieren bei Kindern mit Bruxismus:
- dysfunktionale Familienkonstellationen [64],
- Angst und Angststörungen [92],
- getrennte oder geschiedene Eltern [12],
- berufstätige Mütter [97],
- Schlafstörungen [21],
- Licht und/oder Geräusche im Kinderzimmer [98],
- Ein Elternteil oder beide Eltern von Bruxismus betroffen [63] (51% bei betroffenen Eltern vs. 31% bei Eltern ohne Vorgeschichte).
Bei Kleinkindern, die noch nicht sprechen, kann Schlafbruxismus auch ein Ausdruck von Angst oder Wut sein [15].
SB wurde mit verschiedenen charakteristischen Persönlichkeitsmerkmalen in Verbindung gebracht:
- Angst und Angststörungen [7], [23], [26], [31], [35], [36], [82], [85], [89], [92],
- Stress [31],
- Neurotizismus [26],
- ruheloses Verhalten (Fonseca et al. 2011)
- Fonseca CME, Dos Santos MBF, Consani RLX, et al. Incidence of sleep bruxism among children in Itanhandu, Brazil. Sleep Breath. 2011;15(2):215-220
- PTBS [15],
- Alkohol-, Nikotin- und Drogenkonsum; Passivrauchen [81],
- übermäßiger Kaffeekonsum (>6 Tassen pro Tag) [81],
- häufige Anwendung dentaler Applikationen [101],
- Depressionen [70].
Sozioökomischer Status – Beobachtungsstudien zeigen, dass über die Hälfte der von SB betroffenen Kinder einen niedrigen sozioökonomischen Hintergrund aufweisen [99].
Sozioökomischer Status – Beobachtungsstudien zeigen, dass über die Hälfte der von SB betroffenen Kinder einen niedrigen sozioökonomischen Hintergrund aufweisen [99].
Anatomisch-strukturelle Faktoren – Schlafbruxismus kann durch Verengungen der Atemwege ausgelöst werden. Dabei können plötzliche Microarousals entstehen, welche dann eine Tachykardie stimulieren können. Diese wiederum begünstigt eine rhythmische Aktivität der Kaumuskeln sowie Zähneknirschen, welche die T-Zell-Rezeptoren stimuliert, was letztendlich zu einer Bradykardie führt [24].
Allgemein ist Bruxismus außerdem mit einer nach vorn-unten verschobenen Kopfhaltung assoziiert [101].
Oh et al. fanden in einer aktuellen Studie heraus, dass die Auftrittswahrscheinlichkeit von SB durch die Risikofaktoren vergrößerte Mandeln, eingeschränkte Zungenbeweglichkeit und eingeschränkte Nasenatmung vergrößert wird [80]. Diese steigt zudem, je mehr der 3 Risikofaktoren vorliegen, auf 91% (3 Risikofaktoren) vs. 9% (0 Risikofaktoren).
Genotypische Risikofaktoren – Sequenzvariationen in den Genen, sog. Polymorphismen, insbesondere im HTR2A-Gen, korrelieren mit einem erhöhten Serotonin-vermittelten Risiko für Schlafbruxismus [2], [85], [86], [103], Stress und Angst [27], [32], [42]. Ein systematisches Review identifizierte außerdem einen genetischen Effekt bei WB. So tritt WB insbesondere häufiger bei Bewegungsstörungen auf, die mit Stereotypien einhergehen [29], die durch Angst beeinflusst werden. Neben genetischen Faktoren werden epigenetische Einflussfaktoren diskutiert, da Syndrome wie Rett-Syndrom, Prader-Willi Syndrom und Angelman-Syndrom mit Bruxismus korrelieren [17].
Veränderungen der Biochemie des Gehirns – Bruxismus führt zu einer Erhöhung von Noradrenalin sowie von Katecholamin durch den emotionalen Stress [25], [96]. Weiters erhöhen sich die Spiegel von Glutamat, Dopamin und Gamma-Aminobuttersäure (GABA), während diese Anpassungen teils positive Wirkungen entfalten [49]. Bracha et al. fanden heraus, dass Bruxismus eine erhöhte Signalwirkung in den Noradrenalin-Neuronen des Truncus cerebri bewirkt, v.a. in Kombination mit noch nicht heruntergeregelten Rezeptoren. Serotoninrezeptor-Subtypen spielen dabei eine komplexe Rolle [15]. Insbesondere das Serotonin (5-HT) als Neurotransmitter in Verhaltensreaktionen auf Umweltreize (soziales Verhalten, Gefühlswelt, Schlaf, zirkadianem Rhythmus, Thermoregulation und Stressbewältigungsstrategien) interagiert mit der Aufrechterhaltung der Erregung, Regulierung der Stressreaktion, des Muskeltonus und der Atmung [42], [103]. Dies deutet darauf hin, dass Serotonin eine Rolle bei der SB-Pathogenese spielen könnte [86]. Diese Hypothese wird dadurch bekräftigt, dass Serotonin-Wiederaufnahmehemmer (SSRI) bei anfälligen Personen SB-Episoden auslösen können [61].
Reflux – Die Säureeinwirkung bei Reflux im Ösophagus initiiert Microarousals und rhythmische Kaumuskelaktivitäten, welche durch Stimulation autonomer kortikaler Reflexe entstehen [57]. Mit einer angegebenen Prävalenz von 74% stellt der Reflux eine häufige Komorbidität von Schlafbruxismus dar [45].
Craniomandibuläre Dysfunktionen – Wie oben erwähnt, besteht ein Zusammenhang zwischen CMD und Bruxismus. CMD umfasst verschiedene Störungen des Kiefergelenk-Kausystems zusammen, die charakterisiert sind durch Schmerzen im Kiefergelenk oder in der Kaumuskulatur, durch Funktionseinschränkungen des Kiefers und in assoziierten Geweben (Bänder/Bindegewebsstrukturen) und beim Kauen auftretende Knackgeräusche (de Leeuw et al. 1994). Die Komplexität von Störungsmustern wird durch eine multifaktorielle Krankheitsentstehung bedingt, die traumatologische, anatomische, neuromuskuläre und psychosoziale Faktoren umfasst (Steenks 1991, Winkelmann et al. 1999).
de Leeuw JRJ, Ros WJG, Steenls MH, et al. Multidimensional evaluation of craniomandibular dysfunction. II: Pain assessment. J Oral Rehabil. 1994;21(5):515-532
Steenks MH. Kiefergelenksfehlfunktionen Aus Physiotherapeutischer Und Zahnmedizinischer Sicht: Diagnose Und Therapie. Quintessenz-Verlag-GmbH; 1991
Winkelmann C, Schreiber TU, Weih C, et al. Ansätze zur Physiotherapie bei kraniomandibulären Dysfunktionen. Krankengymn. 1999;51:2042-2054
Bei CMD kommt es häufig zu sekundären, meist temporalen Kopfschmerzen. Canto et al. untersuchten den weiteren Zusammenhang von CMD mit SB. Die Ergebnisse zeigen für Erwachsene mit SB ein mehr als 3-fach erhöhtes Risiko für primären Kopfschmerz [18]. Die Datenlage für Kinder ist nicht ausreichend, um eine Aussage zu treffen. Es wird diskutiert, ob Triggerpunkte in der Nacken-, Schulter- und Kaumuskulatur zu übertragenem Spannungskopfschmerz führen, indem diese Schmerzpunkte zentrale Sensitivierungsprozesse auslösen. Eine Hypothese dazu lautet, dass die Kopfschmerzen über Nozizeptoren der Kaumuskulatur und in den Kiefergelenken induziert werden. Kommt es dann zu Bruxismus, könnte dies zur Reduktion der Reizschwelle des Nucleus spinalis nervi trigemini pars caudalis oder zu einer zentralen Sensitivierung dieses Nervengebietes führen [18].
Pathophysiologie des Schlafbruxismus
Periphere okklusale Faktoren (z.B. Zahnschluss als morphologischer Faktor) spielen eine unterordnete Rolle im Gegensatz zur zentralen Regulation [59], [104] (s.o.). Bei der zentralen Regulation wird noch zwischen pathophysiologische und psychosoziale Faktoren unterschieden [104]. Zu den pathophysiologischen Faktoren gehören u.a. eine anormale Exzitabilität der zentralen motorischen Innervation des Kiefers. Grund hierfür können falsch regulierte Hirnstammhemmungsschaltungen, z.B. von den Hirnnerven V und X, sowie subkortikale Strukturen, sein [33]. Die psychsozialen Risikofaktoren sind oben beschrieben worden.
Während des Schlafs treten pathophysiologische Variationen von Nervenmustern durch den (Para-)Sympathikus auf [79]. Diese verschiedenen Erregungsmuster sind in Abb. 2 dargestellt, die zeitliche Abfolge fasst Abb. 3 zusammen.
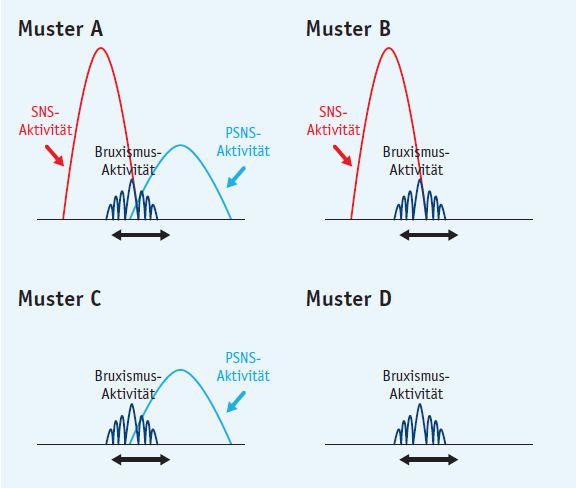
Abb. 2: Einfluss des sympathischen (SNS) und parasympathischen (PSNS) Nervensystems auf den Verlauf des Schlafbruxismus (nach [79]):
- Muster A: Aktivierung des SNS induziert die SB-Aktivität, welche durch eine PSNS-Aktivierung fortgesetzt wird. Die mittlere Anfangszeit des SNS (vor SB-Aktivität) beträgt 11,8 sec; die mittlere Anfangszeit des PSNS (nach Beginn der SB-Aktivität) 10,3 sec.
- Muster B: Aktivierung des SNS induziert die SB-Aktivität, auf die keine Aktivierung des PSNS folgt.
- Muster C: Die SB-Aktivierung erfolgt ohne das SNS, wird aber vom PSNS begleitet.
- Muster D: Die SB-Aktivität startet ohne Beteiligung des SNS oder PSNS.
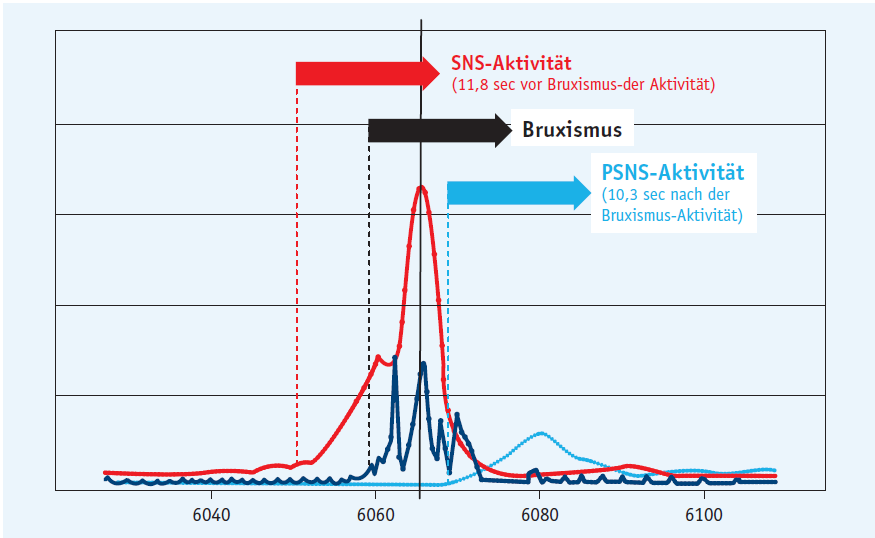
Abb. 3: Darstellung des zeitlichen Zusammenhangs der mittleren Anfangszeit des SNS und PSNS und des Auftretens vom Schlafbruxismus in Sekunden (nach [79])
Neuroevolutionäre und paläoanthropologische Perspektiven
Im Laufe der Evolution (ca. 2 Millionen Jahre bis vor 200.000 Jahren) führte Bruxismus zu einer Stärkung der Masseter- und Temporalismuskulatur und damit auch des Bisses‘. Dies war besonders in der Zeit vor der Entdeckung des Feuers grundlegend für die Nahrungsaufnahme von Pflanzen und führte zu einem Überleben des Homo [15].
Bracha hat im Jahr 2005 zudem die Hypothese aufgestellt, dass das Kieferzusammenpressen zu einem vergrößerten Blutfluss durch die Partes mastiodea des Schläfenbeins führt, was zu einem erhöhten Blutfluss durch die Temporallappenstrukturen unter Beteiligung einer akuten Aktivierung limbischer Angstkreisläufe führen kann [15]. So könnte sich eine alternative stressinduzierte Furchtschaltung, das sog. Freezing oder Erschlaffen durch Vagus-Aktivierung, als ein möglicher Überlebensvorteil als Gegensatz zu der Flucht-oder-Kampf-Reaktion entwickelt haben [13], [16]. Natürlich diente ein starker Biss auch der Verteidigung, und die menschliche Mundflora in Kombination mit einem starken Biss erzeugte eine hohe Sterblichkeitsrate bei Beutetieren und Angriffen [90]. Diese durchaus als positiv zu bewertenden Aspekte des Bruxismus setzten sich in dem adaptiven Zweck, die Zähne scharf zu halten, weiter fort [15].
So kann Bruxismus in der heutigen Zeit auch als eine Manifestation von akuter Angst bzw. chronischer emotionaler Belastung betrachtet werden [15].
Weitere Vorteile des Bruxismus
Zum einen könnte SB eine Schutzfunktion in der Nacht darstellen [41], [58], z.B. in der Aufrechterhaltung der Atmung durch die Unterstützung des Masseters für den M. genioglossus. Dieser wirkt als effizienter Dilatator der oberen Atemwege [46], was zu einer Schmierung des Oropharynx führt [76] und damit den oberen Abschnitt des Verdauungstraktes schützt [49], [76], [100]. Zum anderen führt eine maximale Masseteraktivität zu einer Leistungsverbesserung im Golfsport [94]. Zudem dient ein starker Biss der Selbstverteidigung bei körperlichen und sexuellen Übergriffen [90].
Potenzielle Folgen von Bruxismus
Bei Kindern erfordert SB selten eine Intervention [74] und bringt meistens keine schwerwiegenden Schäden mit sich [91]. Zu den wichtigsten Folgen, die dennoch auftreten können, gehören Zahnzerstörung, Zahnausfall, Kiefergelenk- und Kiefermuskelschmerzen, Einschränkung der Kieferbewegung und primäre Kopfschmerzen (bei 60% der SB-Betroffenen) [8], [40], [44], [93]. Bei gesunden Kindern sind es hingegen nur 31% [12]. Allerdings kann SB zu stressinduzierten Störungen, wie z.B. zum Chronic Fatigue Syndrome und Fibromyalgia führen [1]. Weiters gibt es Korrelationen, jedoch keine Kausalitäten, zwischen der gastroösophagealen Refluxkrankheit, Depressionen, Angststörungen sowie einer verminderten Schlafqualität mit Bruxismus [50].
Diagnostik des Schlafbruxismus
Folgende Symptome und Anzeichen werden von Patient*innen geschildert [77]:
- Schmerzen in den Kiefergelenken, der Kau- und Nackenmuskulatur,
- Kopfschmerzen, vor allem im Bereich der Schläfe beim Aufwachen,
- Überempfindliche Zähne,
- übermäßige Zahnbeweglichkeit ohne feststellbaren zahnärztlichen Grund,
- schlechter Schlaf.
Folgende klinischen Zeichen sind zu finden [77]:
- nicht-kariöser Zahnhartsubstanzverlust und/oder
- Verlust von Restaurationsmaterialien, Rekonstruktionen oder Füllungen,
- Zungen- und Wangenimpressionen,
- weißliche Verhornungsleiste im Planum buccale,
- lokaler Zahnfleischrückgang,
- Hypertonus der Kaumuskulatur,
- Kieferöffnung bzw. -schluss eingeschränkt,
- Torus palatinus oder Tori mandibulares,
- Druckempfindlichkeit sowie eine sichtbare Vergrößerung der Temporalis- und Massetermuskulatur [15].
Weiters lässt sich Bruxismus mehr oder weniger verlässlich anhand verschiedener diagnostischer Herangehensweisen einteilen (mod. nach [88]).
- möglicher WB/SB: positive Hinweise aus Befragung/Fragebögen,
- wahrscheinlicher WB/SB: positive klinische Hinweise mit oder ohne positive Hinweise aus Befragung/Fragebögen,
- definitiver WB/SB: positive instrumentelle Befunde mit oder ohne positive Befunde aus Befragung/Fragebögen und/oder positive klinische Zeichen.
Eine (frühzeitige) Diagnosestellung zur Reduzierung klinischer Zeichen ist von großer Bedeutung. Es sollen nicht-kariöse Zahnhartsubstanzverluste, Verlust von Restaurationsmaterialien, parodontale Probleme, die Entwicklung einer CMD und Kopfschmerzen vermieden werden [88].
Lediglich für den SB wurden durch die American Association of Sleep Medicine (AASM) bereits Kriterien gesammelt, welche die Diagnose SB sichern (Tab. 1) [6].

Tab. 1: Kriterien der American Association for Sleep Medicine (AASM) für schlafassoziierten Bruxismus
Behandlungsansätze
Wie oben beleuchtet, dient der Schlafbruxismus Anpassungsreaktionen und Schutzmechanismen. Mehrere kritische systematische Übersichtsarbeiten fanden für den Zusammenhang zwischen SB und negativen Gesundheitsergebnissen nur eine sehr schwache oder gar keine Evidenz [59], [72], [73]. So kommt Beddis zu dem Schluss, dass es unwahrscheinlich ist, dass Bruxismus keine Funktion hat, und deshalb lediglich bei Problemen aufgrund von SB eine Behandlung stattfinden sollte [10]. Da bei Kindern SB selten zu negativen Auswirkungen führt, werden manualtherapeutische Behandlungsstrategien in dieser Altersgruppe kontrovers diskutiert [95].
Manuelle Behandlungsansätze
Reduzierung des Muskelhypertonus – durch Massage oder/und Dehnung der Kau- und Nackenmuskulatur, z.B. mittels Muskel-Energie-Techniken, können den Bewegungsumfang vergrößern, Schmerzen reduzieren und verbessern die Unterkieferruheposition [102].
Bauchatmung – Generell kann die Zwerchfellatmung bis in den Bauch trainiert werden; ggf. können Zwerchfelldysfunktionen und assoziierte Organdysfunktionen (z.B. Magen, Leber, Lunge, Herz etc.) behoben werden.
Entspannungsförderung – durch entspannende Aktivitäten, z.B. durch Visualisierung von Bildern oder bewusstes Entspannen verschiedener Muskelgruppen [84] oder durch vagusstimulierende Interventionen [55], [56].
LEIT-Reset – Extrinsische und intrinsische Kiefertechniken werden aufeinander abgestimmt angewendet (Liem extrinsisches und intrinsisches TMG-Reset):
Extrinsische durch Behandler*innen ausgeführte Techniken:
- Myofasziale Release-Techniken und Triggerpunktbehandlung: insbesondere der Kau-, Hyoid- und Nacken- und Schultermuskeln.
- Techniken für Kiefergelenk und assoziierte Strukturen wie Band-Kapsel-Apparat [52].
- Körperhaltung: Behandlung auf- und absteigender Muskelketten [52].
- Neuromuskuläre Inhibitionstechniken: z.B. des aufsteigenden retikulären Aktivierungssystems (ARAS), Afferenzen der Hirnnerven (insbesondere V, VII, IX, X), des Hinterhorns im Rückenmark und somatischer Nerven.
- Techniken für das autonome Nervensystem: z.B. Inhibitionstechniken des Sympathikus und Vagusnerv-stimulierende Techniken [55], [56].
- Bei Reflux: Technik für den unteren Ösophagusspinkter [28].
- Bei Verengung der Atemwege: Mobilisierung des Thorax und der Atemwege und Atemtechniken [9].
- Bei vergrößerten Mandeln: lymphatische Stimulation der Rachen-, Kopf-, Halsregion [51], [52], Ernährungsumstellung [56].
- Bei eingeschränkter Zungenbeweglichkeit: Behandlung von Dyskinesien, Zungenmobilisation [52].
- Bei emotionaler Belastung, Angst: Behandlung mittels Ansätze der psychosomatischen Osteopathie, z.B. multimodaler bifokaler Integration [53], [54].
Intrinsische von den Betroffenen ausgeführte Selbsthilfetechniken:
- Kau-, Hyoid-, Nackenmuskeltechniken, z.B. mit alternierender An- und Entspannung oder reine Muskelentspannungsübungen wie „Kiefer hängen lassen“ oder/und reziproke Spannungsinhibitionstechniken der Muskulatur [52].
- Atemübungen: insbesondere verlangsamte Bauchatmung mit der Zunge am Gaumen [56].
- Körperhaltungsübungen, z.B. zur Korrektur der Kopf-/Nackenposition.
- Myofasziale Vibrationstechniken im Liegen und Sitzen.
- Bei Einschränkung der Zungenbeweglichkeit und vergrößerten Mandeln: Anwendung des Faceformers: Patient*innen, die mit FaceFormer trainiert hatten, wurden mit solchen, die mit Knirscherschienen versorgt wurden, verglichen. Bei Schienenpatient*innen gab es keine Verbesserungen, sondern Verstärkung des Knirschens/Pressens, während die Faceformer-Gruppe bereits nach 8 Wochen eine signifikante Verbesserung zeigte [11].
- Entspannungsübungen, vagusnervstimulierende Selbstübungen und HRV (Herzratenvariabilität)-Biofeedback [56].
- Angstreduzierende Selbstübungen.
Literatur zu:
Liem T. Bruxismus und Osteopathie. Osteopathische Medizin 2022; 2:
Literatur
- Aaron LA, Buchwald D. A review of the evidence for overlap among unexplained clinical conditions. Ann Intern Med. 2001; 134 (9_Part_2): 868–881
- Abe Y, Suganuma T, Ishii M et al. Association of genetic, psychological and behavioral factors with sleep bruxism in a Japanese population. J Sleep Res. 2012; 21 (3): 289–296
- Ahlberg K, Jahkola A, Savolainen A et al. Associations of reported bruxism with insomnia and insufficient sleep symptoms among media personnel with or without irregular shift work. Head Face Med. 2008; 4 (1): 1–6
- Alencar NA de, Fernandes ABN, Souza MMG de et al. Lifestyle and oral facial disorders associated with sleep bruxism in children. CRANIO®. 2017; 35 (3): 168–174
- Alfano CA, Bower JL, Meers JM. Polysomnography-detected bruxism in children is associated with somatic complaints but not anxiety. J Clin Sleep Med. 2018; 14 (1): 23–29
- American Association of Sleep Medicine (AASM). International classification of sleep disorders. Diagnostic coding Man. Published online 2005: 51–55
- Alves AC, Alchieri JC, Barbosa GAS. ACTA-1–2013-final_3–2011. Published online 2013
- Bader G, Lavigne G. Sleep bruxism; an overview of an oromandibular sleep movement disorder. Sleep Med Rev. 2000; 4 (1): 27–43
- Benjamin JG, Moran RW, Plews DJ, Kilding AE, Barnett LE, Verhoeff WJ, Bacon CJ. The effect of osteopathic manual therapy with breathing retraining on cardiac autonomic measures and breathing symptoms scores: A randomised wait-list controlled trial. J Bodyw Mov Ther. 2020 Jul; 24 (3): 282–292
- Beddis H, Pemberton M, Davies S. Sleep bruxism: an overview for clinicians. Br Dent J. 2018; 225 (6): 497–501
- Berndsen KJ, Berndsen S, Kopp ST. New ways of functional treatment of bruxism Face Former Therapy. Journal Orofacial Orthopedics. 2009; 70: 420
- Bortoletto CC, Salgueiro M da CC, Valio R et al. The relationship between bruxism, sleep quality, and headaches in schoolchildren. J Phys Ther Sci. 2017; 29 (11): 1889–1892
- Bracha BHS. 2004_bracha -FEAR–Freeze_Flight_Fight_Fright_Faint. 2004; 9 (9): 679–685
- Bracha HS, Bracha AS, Williams AE et al. The human fear-circuitry and fear-induced fainting in healthy individuals: The paleolithic-threat hypothesis. Clin Auton Res. 2005; 15 (3): 238–241
- Bracha HS, Ralston TC, Williams AE et al. The clenching-grinding spectrum and fear circuitry disorders: Clinical insights from the neuroscience/paleoanthropology interface. CNS Spectr. 2005; 10 (4): 311–318
- Bracha HS, Ralston TC, Matsukawa JM et al. Does " Fight or Flight" Need Updating? 2004; (October)
- Čalić A, Peterlin B. Epigenetics and Bruxism: Possible Role of Epigenetics in the Etiology of Bruxism. Int J Prosthodont. 2015; 28 (6)
- Canto G, Singh V, Bigal M et al. Association Between Tension-Type Headache and Migraine with Sleep Bruxism: A Systematic Review. Headache. 2014; 54
- Carlsson GE, Egermark I, Magnusson T. Predictors of bruxism, other oral parafunctions, and tooth wear over a 20-year follow-up period. J Orofac Pain. 2003; 17 (1)
- Castrillon EE, Ou K-L, Wang K et al. Sleep bruxism: an updated review of an old problem. Acta Odontol Scand. 2016; 74 (5): 328–334
- Castroflorio T, Bargellini A, Rossini G et al. Risk factors related to sleep bruxism in children: A systematic literature review. Arch Oral Biol. 2015; 60 (11): 1618–1624
- Castroflorio T, Bargellini A, Rossini G et al. Sleep bruxism in adolescents: a systematic literature review of related risk factors. Eur J Orthod. 2017; 39 (1): 61–68
- Cheifetz AT, Osganian SK, Allred EN et al. Associated Correlates in Children as Reported by Parents. J Dent Child. 2005; 72 (2): 67–73
- Chowdhury T, Bindu B, Singh GP et al. Sleep disorders: Is the trigemino-cardiac reflex a missing link? Front Neurol. 2017; 8 (FEB): 1–7
- Clark GT, Rugh JD, Handelman SL. Nocturnal Masseter Muscle Activity and Urinary Catecholamine Levels in Bruxers. J Dent Res. 1980; 59 (10): 1571–1576
- Cruz-Fierro N, Martínez-Fierro M, Cerda-Flores RM et al. The phenotype, psychotype and genotype of bruxism. Biomed Reports. 2018; 8 (3): 264–268
- Donnellan MB, Burt SA, Levendosky AA et al. Genes, personality, and attachment in adults: A multivariate behavioral genetic analysis. Personal Soc Psychol Bull. 2008; 34 (1): 3–16
- Eguaras N, Rodríguez-López ES, Lopez-Dicastillo O, Franco-Sierra MÁ, Ricard F, Oliva-Pascual-Vaca Á. Effects of Osteopathic Visceral Treatment in Patients with Gastroesophageal Reflux: A Randomized Controlled Trial. J Clin Med. 2019 Oct 19; 8 (10): 1738
- Ella B, Ghorayeb I, Burbaud P et al. Bruxism in movement disorders: a comprehensive review. J Prosthodont. 2017; 26 (7): 599–605
- Every RG. Significance of tooth sharpness for mammalian, especially primate, evolution. Contrib Primatol. 1975; 5: 293–325
- Ferreira-Bacci A do V, Cardoso CLC, Díaz-Serrano KV. Behavioral problems and emotional stress in children with bruxism. Braz Dent J. 2012; 23 (3): 246–251
- Fraley RC, Roisman GI, Booth-LaForce C et al. Interpersonal and genetic origins of adult attachment styles: a longitudinal study from infancy to early adulthood. J Pers Soc Psychol. 2013; 104 (5): 817
- Gastaldo E, Member S, Quatrale R et al. Bruxism Centrally Mediated-not occlusion. Published online 2005: 145–155
- Giraki M, Schneider C, Schäfer R et al. Correlation between stress, stress-coping and current sleep bruxism. Head Face Med. 2010; 6 (1)
- Gorayeb MAM, Gorayeb R. Cefaléia associada a indicadores de transtornos de ansiedade em uma amostra de escolares de Ribeirão Preto, SP. Arq Neuropsiquiatr. 2002; 60 (3B): 764–768
- Gungormus Z, Erciyas K. Evaluation of the relationship between anxiety and depression and bruxism. J Int Med Res. 2009; 37 (2): 547–550
- Guo H, Wang T, Niu X et al. The risk factors related to bruxism in children: A systematic review and meta-analysis. Arch Oral Biol. 2018; 86: 18–34
- Insana SP, Gozal D, McNeil DW et al. Community based study of sleep bruxism during early childhood. Sleep Med. 2013; 14 (2): 183–188
- Jokubauskas L, Baltrušaitytė A. Relationship between obstructive sleep apnoea syndrome and sleep bruxism: a systematic review. J Oral Rehabil. 2017; 44 (2): 144–153
- Kato T, Lavigne GJ. Sleep Bruxism: A Sleep-Related Movement Disorder. Sleep Med Clin. 2010; 5 (1): 9–35
- Khoury S, Rouleau GA, Rompré PH et al. A significant increase in breathing amplitude precedes sleep bruxism. Chest. 2008; 134 (2): 332–337
- Kiser D, SteemerS B, Branchi I et al. The reciprocal interaction between serotonin and social behaviour. Neurosci Biobehav Rev. 2012; 36 (2): 786–798
- Kleinberg I. Bruxism: aetiology, clinical signs and symptoms. Aust Prosthodont J. 1994; 8: 9–17
- Knutson GA. Vectored upper cervical manipulation for chronic sleep bruxism, headache, and cervical spine pain in a child. J Manipulative Physiol Ther. 2003; 26 (6): 395
- Kuhn M, Türp JC Risikofaktoren für Bruxismus–Eine Literaturübersicht von 2007 bis 2016. Swiss Dent J. 2018; 128: 125–129
- Landry M-L, Rompré PH, Manzini C et al. Reduction of sleep bruxism using a mandibular advancement device: an experimental controlled study. Int J Prosthodont. 2006; 19 (6)
- Lavigne GJ, Khoury S, Abe S et al. Bruxism physiology and pathology: An overview for clinicians. J Oral Rehabil. 2008; 35 (7): 476–494
- Lavigne GJ, Rompré PH, Poirier G et al. Rhythmic masticatory muscle activity during sleep in humans. J Dent Res. 2001; 80 (2): 443–448
- Lavigne GJ, Introduction I. Neurobiological mechanisms involved in sleep bruxism. Crit Rev Oral Biol Med. 2003; 14 (1): 30–46
- Li Y, Yu F, Niu L et al. Association between bruxism and symptomatic gastroesophageal reflux disease: A case-control study. J Dent. 2018; 77 (July): 51–58
- Liem T. Update zur Drainage des Gehirns und osteopathische Behandlungsansätze, Osteopathische Medizin 2017; 18 (2), 22–27
- Liem T. Praxis Der Kraniosakralen Osteopathie. 4. überarbeitete und erw. Auflage. Thieme, Stuttgart, 2020
- Liem T. Neuhuber W. Osteopathic Treatment Approach to Psychoemotional Trauma by Means of Bifocal Integration: clinical practice, Journal of the American Osteopathic Association 2020a; 120 (3), 1–10
- Liem T. Neuhuber W. Psychosomatische Osteopathie bei Trauma am Beispiel der bifokalen Integration. Osteop Med. 2020b; 21 (4): 6–13
- Liem T. Vagusaktivierung und Stressreaktion aus Sicht der Osteopathie. Osteopat Medizin. 2021; 22 (4): 10–15
- Liem T, Tsolodimos C. Das Osteopathie-Selbsthilfe-Buch. Wie Osteopathie Wirkt Und Die Selbstheilung Fördert. Mit Übungen Für Jeden Tag. Trias, Stuttgart; 2022
- Lobbezoo F, Ahlberg J, Manfredini D et al. Are bruxism and the bite causally related? J Oral Rehabil. 2012; 39 (7): 489–501
- Lobbezoo F, Ahlberg J, Glaros AG et al. Bruxism defined and graded: An international consensus. J Oral Rehabil. 2013; 40 (1): 2–4
- Lobbezoo F, Ahlberg J, Raphael KG et al. International consensus on the assessment of bruxism: Report of a work in progress. J Oral Rehabil. 2018; 45 (11): 837–844
- Lobbezoo F, Rompré PH, Soucy JP et al. Lack of Associations between Occlusal and Cephalometric Measures, Side Imbalance in Striatal D2 Receptor Binding, and Sleep-Related Oromotor Activities. J Orofac Pain. 2001; 15 (1): 64–71
- Lobbezoo F, Van Denderen RJA, Verheij JGC et al. Reports of SSRI-Associated Bruxism in the Family Physician’s Office. J Orofac Pain. 2001; 15 (4): 340–346
- Lobbezoo F, van der Zaag J, Naeije M. Bruxism: its multiple causes and its effects on dental implants–an updated review. J Oral Rehabil. 2006; 33 (4): 293–300
- Lobezzo F, Visscher CM, Ahlberg J et al. Bruxism and genetics: a review of the literature -. J Oral Rehabil. 2014; 41: 709—714
- Lurie O, Zadik Y, Einy S et al. Bruxism in military pilots and non-pilots: tooth wear and psychological stress. Aviat Space Environ Med. 2007; 78 (2): 137–139
- Machado E, Dal-Fabbro C, Cunali PA et al. Prevalence of sleep bruxism in children: A systematic review. Dental Press J Orthod. 2014; 19 (6): 54–61
- Maluly M, Andersen ML, Dal-Fabbro C et al. Polysomnographic study of the prevalence of sleep bruxism in a population sample. J Dent Res. 2013; 92 (7_suppl): S97-S103
- Manfredini D, Arreghini A, Lombardo L et al. Assessment of anxiety and coping features in bruxers: a portable electromyographic and electrocardiographic study. J Oral Facial Pain Headache. 2016; 30 (3): 249–254
- Manfredini D, Bracci A, Djukic G. BruxApp: the ecological momentary assessment of awake bruxism. Minerva Stomatol. 2016; 65 (4): 252–255
- Manfredini D, Bucci MB, Sabattini VB et al. Bruxism: overview of current knowledge and suggestions for dental implants planning. CRANIO®. 2011; 29 (4): 304–312
- Manfredini D, Fabbri A, Peretta R et al. Influence of psychological symptoms on home‐recorded sleep‐time masticatory muscle activity in healthy subjects. J Oral Rehabil. 2011; 38 (12): 902–911
- Manfredini D, Lobbezoo F. Role of psychosocial factors in the etiology of bruxism. J Orofac pain. 2009; 23 (2): 153–166
- Manfredini D, Lobbezoo F. Relationship between bruxism and temporomandibular disorders: A systematic review of literature from 1998 to 2008. Oral Surgery, Oral Med Oral Pathol Oral Radiol Endodontology. 2010; 109 (6): e26-e50
- Manfredini D, Poggio CE, Lobbezoo F Is bruxism a risk factor for dental implants? A systematic review of the literature. Clin Implant Dent Relat Res. 2014; 16 (3): 460–469
- Manfredini D, Restrepo C, Diaz‐Serrano K et al. Prevalence of sleep bruxism in children: a systematic review of the literature. J Oral Rehabil. 2013; 40 (8): 631–642
- Marthol H, Reich S, Jacke J et al. Enhanced sympathetic cardiac modulation in bruxism patients. Clin Auton Res. 2006; 16 (4): 276–280
- Miyawaki S, Lavigne GJ, Mayer P et al. Association between sleep bruxism, swallowing-related laryngeal movement, and sleep positions. Sleep. 2003; 26 (4): 461–465
- Murali R V, Rangarajan P, Mounissamy A Bruxism: Conceptual discussion and review. J Pharm Bioallied Sci. 2015; 7 (Suppl 1): S265
- Murray CG, Sanson GD. Thegosis‐A critical review. Aust Dent J. 1998; 43 (3): 192–198
- Nukazawa S, Yoshimi H, Sato S. Autonomic nervous activities associated with bruxism events during sleep. CRANIO®. 2018; 36 (2): 106–112
- Oh JS, Zaghi S, Ghodousi N et al. Determinants of probable sleep bruxism in a pediatric mixed dentition population: a multivariate analysis of mouth vs. nasal breathing, tongue mobility, and tonsil size. Sleep Med. 2021; 77: 7–13
- Ohayon MM, Li KK, Guilleminault C. Risk factors for sleep bruxism in the general population. Chest. 2001; 119 (1): 53–61
- de Oliveira MT, Bittencourt ST, Marcon K et al. Sleep bruxism and anxiety level in children. Braz Oral Res. 2015; 29 (1): 1–5
- Olmos SR. Comorbidities of chronic facial pain and obstructive sleep apnea. Curr Opin Pulm Med. 2016; 22 (6): 570–575
- Ommerborn MA, Schneider C, Giraki M et al. Effects of an occlusal splint compared with cognitive‐behavioral treatment on sleep bruxism activity. Eur J Oral Sci. 2007; 115 (1): 7–14
- Oporto Gh, Bornhardt T, Iturriaga V et al. Genetic polymorphisms in the serotonergic system are associated with circadian manifestations of bruxism. J Oral Rehabil. 2016; 43 (11): 805–812
- Oporto GH, Lagos JD, Bornhardt T et al. ¿ Es posible la contribución de factores genéticos en el bruxismo? Int J Odontostomatol. 2012; 6 (3): 249–254
- Ortiz MI, Rangel-Barragán RO, Contreras-Ayala M et al. Procedural pain and anxiety in pediatric patients in a Mexican dental clinic. Oral Health Dent Manag. 2014; 13 (2): 495–501
- Peroz I, Bernhardt O, Kares H et al. S3-Leitlinie (Langversion) Diagnostik und Behandlung von Bruxismus. Zeitschrift für Kraniomandibuläre Funktion. 2019; 11 (3): 225-i385
- Petit D, Touchette É, Tremblay RE et al. Dyssomnias and parasomnias in early childhood. Pediatrics. 2007; 119 (5)
- Pretty IA, Hall RC. Forensic dentistry and human bite marks: issues for doctors. Hosp Med. 2002; 63 (8): 476–482
- Reddy SV, Kumar M, Sravanthi D. Bruxism: A Literature Review. J Int Oral Heal. 2014; 6 (6): 105–109
- Restrepo CC, Vásquez LM, Alvarez M et al. Personality traits and temporomandibular disorders in a group of children with bruxing behaviour. J Oral Rehabil. 2008; 35 (8): 585–593
- Restrepo C, Gómez S, Manrique R. Treatment of bruxism in children: a systematic review. Quintessence Int. 2009; 40 (10): 849–855
- Ringhof S, Hellmann D, Meier F et al. The effect of oral motor activity on the athletic performance of professional golfers. Front Psychol. 2015; 6 (JUN): 1–10
- Santos C, Amorim M, Ferreira E et al. Ejjectivenesss of two. Published online 2014: 1–8
- Seraidarian P, Seraidarian PI, das Neves Cavalcanti B et al. Urinary levels of catecholamines among individuals with and without sleep bruxism. Sleep Breath. 2009; 13 (1): 85–88
- Seraj B, Shahrabi M, Ghadimi S et al. The prevalence of bruxism and correlated factors in children referred to dental schools of Tehran, based on parent’s report. Iran J Pediatr. 2010; 20 (2): 174
- Serra-Negra JM, Paiva SM, Fulgêncio LB et al. Environmental factors, sleep duration, and sleep bruxism in Brazilian schoolchildren: a case-control study. Sleep Med. 2014; 15 (2): 236–239
- Serra-Negra JM, Paiva SM, Seabra AP et al. Prevalence of sleep bruxism in a group of Brazilian schoolchildren. Eur Arch Paediatr Dent. 2010; 11 (4): 192–195
- Thie NMR, Kato T, Bader G et al. The significance of saliva during sleep and the relevance of oromotor movements. Sleep Med Rev. 2002; 6 (3): 213–227
- Vélez AL, Restrepo CC, Peláez‐Vargas A et al. Head posture and dental wear evaluation of bruxist children with primary teeth. J Oral Rehabil. 2007; 34 (9): 663–670
- Visscher CM, Lobbezoo F, Naeije M. Treatment of bruxism: physiotherapeutic approach. Ned Tijdschr Tandheelkd. 2000; 107 (7): 293–296
- Wilhelm K, Siegel JE, Finch AW et al. The long and the short of it: Associations between 5-HTT genotypes and coping with stress. Psychosom Med. 2007; 69 (7): 614–620
- Yap AUJ, Chua AP. Sleep bruxism: Current knowledge and contemporary management. J Conserv Dent. 2016; 19 (5): 383–389